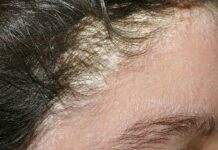
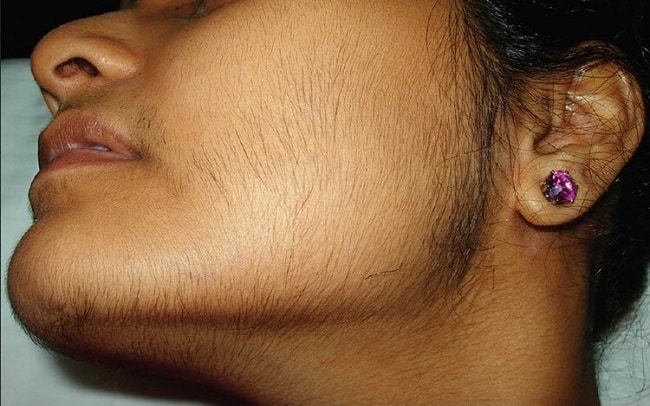
Основным протективным антигеном вируса простого герпеса типа I и II (ВПГ-1, ВПГ-2) является гликопротеин Д (gD), и в меньшей степени — гликопротеин B(gB).
Очищенный gD ВПГ-1 или ВПГ-2 защищает мышей от летальной дозы как ВПГ-1, так и ВПГ-2; стимулирует образование ВН-антител, пассивное введение которых защищает мышей от летальной инфекции ВПГ; стимулирует комплементзависимую и опосредованную антителами цитотоксичность. Комбинация обоих гликопротеинов (gD и gB) усиливает протективную активность препарата. В четырех антигенных участках gD ВПГ-1 различают по крайней мере шесть эпитопов. Антитела к большинству из них нейтрализуют вирус без участия комплемента и подавляют проникновение вируса в клетку. Нейтрализация вируса и индукция протективного иммунитета приводили к активизации гуморальных и клеточных факторов иммунитета у мышей и кроликов, повышали их резистентность к экспериментальному заражению и снижали количество клеток ганглия тройничного нерва, несущих геном вируса. Нейтрализация вируса и индукция протективного иммунитета связаны с аминокислотными остатками 233-259, а адсорбция вируса — с областью в пределах первых 182 аминокислот. Точечные мутации в сайте нейтрализации gD могут сделать его нечувствительным к действию ВН-антител.
Слияние вирусной и клеточной оболочек ВПГ-1 определяет gB. За аналогичные функции вируса Эпштейн-Барра ответственны два гликопротеина (220/200 и 350/300 кД), расположенные на поверхности вириона. Эти белки вызывали у кроликов образование антител, реагирующих с одними и теми же белками на поверхности вирионов и инфицированных вирусом клеток. Вакцина, содержащая гликопротеин 340 кД, вызывала иммунитет у обезьян. В нейтрализации цитомегаловируса и выработке нейтрализующих антител основная роль принадлежит гликопротеинам 86 и 130/55 кД.
В оболочке вируса псевдобешенства (ВПБ) различают три основных гликопротеина (gE, gB, gX), кодируемых u-сегментом вирусного генома. При иммунном ответе свиней на инфекцию защитные антитела формируются к двум гли-копротеинам: gE и gB. Гликопротеин gE состоит из двух субъединиц с массой около 80 кД. Он не является существенным для репликации, поскольку известны вакцинные штаммы с делениями в этой области генома. N-концевой фрагмент gE содержит высокоантигенный домен, способный вызвать образование НВ-антител и защитный эффект. Делеция по гену gE может привести к снижению иммунногенности, чего не наблюдается при удалении гена gX. Предшественники gII и gIII имеют соответственно молекулярную массу 110 и 60 кД. За слияние вирусной и клеточной оболочек и проникновение вируса в клетку ответственен gB. Антигенного дрейфа в gB и gE не обнаружено.
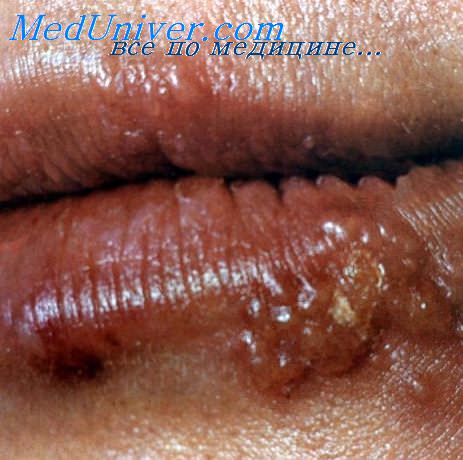
Однако основную роль в индукции синтеза нейтрализующих антител ВПБ, проявляющих активность в отсутствие комплемента, играет gB. Являясь мультифункциональным белком, он, кроме того, играет важную роль в адсорбции и эффективной репликации вируса в культуре клеток. Антитела к gIII обладали более выраженным защитным эффектом у мышей (90-100%) и свиней (84-100%), чем к gII. Гликопротеин gIII играет определяющую роль в клеточном иммунитете, поскольку является главным антигеном-мишенью для вирусспецифических цитотоксических Т-лимфоцитов. Кроме gill, заметная роль в защите вакцинированных животных принадлежит g50 кД, который также является основной мишенью ВН-антител. Следует отметить, что пассивная защита поросят не предотвращала репликацию и экскрецию ВПБ в назофаренгиальной области зараженных животных. Титр нейтрализующих антител in vitro не всегда коррелировал с защитой животных.
Так как все полевые штаммы ВПБ содержат gE, а большинство аттенуированных штаммов, используемых в качестве живых вакцин, не содержат gE, появилась возможность использовать ИФА для дифференциации иммунных и инфицированных животных и тем самым способствовать оздоровлению хозяйств на основе вакцинопрофилактики. Указанная стратегия успешно реализуется в практических условиях в Западной Европе.
За индукцию синтеза ВН-антител герпесвируса типа I крупного рогатого скота (ГВ I) ответственны четыре гликопротеина оболочки. Главными из них являются g70 и g97. Эти гликопротеины содержат основные эпитопы нейтрализации вируса. Гемагглютинирующая активность ГВ крупного рогатого скота связана с мажорным g97, расположенным в шипиках вириона. Главные нейтрализующие эпитопы расположены на гемагглютинирующем домене, что свидетельствует о перспективности использования гемагглютинирующего антигена ГВ 1 крупного рогатого скота для приготовления субъединичной вакцины, 15381. ГВ1 крупного рогатого скота так же, как герпесвирус типа I кошек (ГВК1), агглютинирует эритроциты мышей, хотя гемагглютинирующие домены этих вирусов не идентичны.
В структуре gIV ГВ1 крупного рогатого скота идентифицированы три нейтрализующих домена. Домен I содержит два перекрывающихся эпитопа, домен III — четыре идентичных или перекрывающихся эпитопа, домен II — один эпитоп. Домен I имеет отношение к проникновению вируса в клетки-мишени. Прикрепление вируса к клеткам in vitro опосредовано его главными гликопротеинами, которые в этом отношении можно расположить в ряду gill > gl > gIV. Очищенный gIII полностью блокирует адсорбцию полевого штамма ГВ1 крупного рогатого скота.
В становление гуморального и клеточного иммунитетов свой вклад вносят гликопротеины оболочки gI gIII и особенно gIV. Максимальную защиту телят в экспериментальных условиях обеспечивал gIV, а также безвирусный лизат инфицированных клеток.
Нейтрализующие антитела к трем оболочечным гликопротеинам (gI, gIII и gIV) FBI крупного рогатого скота вводили телятам и определяли защитный эффект при экспериментальном заражении гомологичным вирусом. У привитых животных титры антител в носовом секрете и смывах с конъюнктивы были аналогичны таковым у реконвалесцентов. Несмотря на клинический эффект от введения антител, они не предотвращали размножение ГВ1 крупного рогатого скота в слизистой оболочке носа и глаз, а также не сокращали его экскрецию. Цитотоксические Т-лимфоциты крупного рогатого скота, индуцированные ГВ1 крупного рогатого скота, проявляют специфичность, то есть реагируют только на клетки, экспрессирующие гомологичный или родственный антиген. Мутант ГВ1 крупного рогатого скота с делецией гена gIII не теряет способности размножаться в культуре клеток. Его функциональная дефектность проявляется в замедленной адсорбции и репликации, а также в снижении выхода внеклеточного вируса. По аналогии с вирусом псевдобешенства идентифицированы и делетированы несущественные гены с целью получения аттенуированных «маркированных» вакцин.
]]>