Особенностью всех вирусов герпеса является их способность переходить в латентное состояние и существовать в ядрах клеток (нейронов или клеток крови) в виде латентно-ассоциированных транскриптов. Вирус опоясывающего герпеса может длительное время сохраняться в ядрах клеток чувствительных ганглиев краниальных нервов и межпозвоночных узлов, где происходит транскрипция определенных регионов генома вируса. Активация латентного вируса опоясывающего герпеса происходит на фоне нарушения иммунитета (в результате онкологического процесса, приема иммунодепрессантов и других причин). Развитие устойчивого болевого синдрома после перенесенной герпес-зостерной инфекции, как правило, ассоциировано с возрастом. Этот факт объясняется тем, что в процессе естественного старения происходит уменьшение количества толстых миелинизированных волокон типа А в проводниках. При этом в острой стадии герпетической инфекции в связи с распространением вируса по периневральным пространствам преимущественно поражаются именно волокна типа А, способные активировать нейроны 2-й пластины Рекседа (желатинозной субстанции) задних рогов спинного мозга. В результате снижения активности нейронов желатинозной субстанции их ингибирующее влияние на спинальный уровень модуляции боли («воротный контроль») значительно снижается, что и является ведущим фактором хронизации боли при зостерном поражении у лиц пожилого возраста [1].
В случае манифестации латентной инфекции одновременно поражаются несколько чувствительных ганглиев. Клиническая картина определяется локализацией первичного очага в нервной системе. Описаны следующие формы поражения нервной системы вирусом опоясывающего герпеса:
- общеинфекционная;
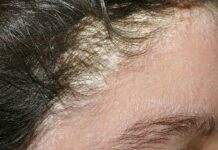
- кожная (пузырьковые высыпания с прозрачным и/или геморрагическим содержимым по ходу пораженных нервов);
- нейропатическая (преобладание в клинической картине нейропатической боли).
В первой стадии заболевания отмечаются общеинфекционные проявления: повышение температуры тела, общая слабость, мышечные боли. На второй стадии появляются пузырьковые высыпания на коже в соответствии с зонами иннервации пораженных ганглиев, отечность кожных покровов. Содержимое пузырьков может быть прозрачным
и/или геморрагическим. Больные жалуются на постоянные боли средней интенсивности (4–6 баллов ВАШ) в зоне иннервации соответствующего нерва. При поражении узла тройничного нерва боли локализуются в зоне иннервации первой ветви (область лба и волосистой части головы до венечного шва, верхнее веко, при наличии высыпаний на роговице – область глазного яблока), на фоне которых отмечаются болевые пароксизмы. Обычно боли менее интенсивны, чем при тригеминальной невралгии, но отличаются длительным (годы) упорным течением. В случае распространения вирусной инфекции на узел коленца лицевого нерва боли и высыпания локализуются в области ушной раковины, наружного слухового прохода и в полости рта (синдром Рамсея Ханта), с последующим развитием паралича мимических мышц. При поражении межпозвоночных узлов кожные проявления и болевой синдром соответствуют зонам их иннервации. Третья стадия герпес-зостерной инфекции – нейропатическая – развивается после рубцевания кожных высыпаний (обычно через 3–4 недели). В зависимости от сроков формирования устойчивого болевого синдрома различают ранние (до 3 месяцев после острого периода) или поздние (более чем через 3 месяца по прошествии острого периода) формы постгерпетической нейропатической боли.
При клинико-неврологическом обследовании определяется нарушение всех видов чувствительности в зоне иннервации соответствующего нерва или корешка с элементами гиперпатии и аллодинии. У части больных имеются триггерные зоны, которые при поражении тройничного нерва в большинстве случаев локализуются на волосистой части головы. Наличие в клинической картине признаков морфологического повреждения ноцицептивной системы (гиперпатия, аллодиния) свидетельствуют о том, что болевой синдром при постгерпетической нейропатии следует расценивать как периферическую форму нейропатической боли. Отличительной особенностью болевого синдрома при постгерпетической нейропатии является наличие флюктуаций интенсивности боли в зависимости от климатических условий и эмоционального состояния больного. Кроме того, у большинства больных с хроническим течением заболевания отмечаются расстройства эмоциональной сферы в виде тревоги, ипохондрии и депрессии.
В случае распространения герпетической инфекции из первичного очага (ганглий) на оболочечные и мозговые сосуды с развитием некротизирующего гранулематозного ангиита нарушается кровообращение в соответствующих областях головного мозга с исходом в инфаркт. При поражении тройничного узла чаще развивается инфаркт затылочных долей или мозжечка; шейных узлов – инфаркт ствола головного мозга. Временной период от момента развития ганглионейропатии до гемипареза составляет от 1 до 7 недель.
В острой стадии заболевания показано как можно более раннее применение противовирусных препаратов [1, 2, 3]. Ацикловир назначают внутривенно капельно по 10 мг/кг массы тела каждые 8 часов в течение 5 дней и 3 дней после прекращения высыпаний или перорально по 800 мг 4 раза в день (длительность курса такая же, как и при внутривенном введении).
Установлено, что медиаторами боли на спинальном уровне являются нейропептиды (субстанция Р, холецистокинин, соматостатин, глютамат), избыточное выделение которых поддерживает интенсивность ноцицептивного потока, усиливает выраженность и продолжительность боли. В последние годы для лечения постгерпетической ганглионейропатии применяется препарат амантадина сульфат (ПК-Мерц) в виде инфузии, который обладает противовирусной и противоболевой активностью. Амантадина сульфат действует как неконкурентный антагонист NMDA-рецепторов нейронов, блокируя передачу патологических глутаматергических импульсов, что способствует уменьшению выраженности болевого синдрома (рис. 1). Эффективность препарата доказана как в острой стадии процесса, так и после заживления высыпаний [2]. Инфузии ПК-МЕРЦ следует назначать внутривенно капельно 2 раза в день в течение 10–14 дней вне зависимости от остроты процесса и выраженности болевого синдрома. После окончания курса внутривенных вливаний рекомендуется прием таблетированного амантадина сульфата 300–600 мг в сутки в течение 2–3 недель с последующим снижением дозы на 100 мг каждые 3 дня до полной отмены препарата.
В хронической стадии постгерпетической ганглионейропатии показано комплексное лечение нейропатической боли с применением противоэпилептических препаратов (карбамазепин 600–800 мг/сут, габапентин 1500–2400 мг/сут) в сочетании с антидепрессантами различных фармакологических групп [1, 2, 3]. С учетом патогенетических механизмов формирования болевого синдрома при постзостерной нейропатии возможно назначение амантадина сульфата в суточной дозе 200 мг в комплексной терапии противоэпилептическими препаратами и антидепрессантами в течение 3 недель. Эффективны также физиотерапевтические методики: электростимуляция, ЧЭНС, иглорефлексотерпия, лазеромагнитотерапия [2].
]]>